Kaltes Licht
Cryo-Fluoreszenzanalytik – Eine innovative Technik für die Wissenschaft
Ein spektroskopischer Tieftemperaturmessplatz weist am Helmholz-Zentrum Dresden-Rossendorf schnell und sensitiv Schwermetalle in diversen Umweltproben nach.
Fluoreszenzmikroskopische und fluoreszenzspektroskopische Untersuchungen finden in der Chemie, Biochemie, Biologie, Medizin, Materialprüfung sowie in den Geowissenschaften eine breite Anwendung. Dabei spielt die chemische Charakterisierung und die Lokalisierung der verschiedensten Analyte/Fluorophore (Schwermetalle, Biomarker) mittels analytischer und bildgebender Verfahren eine wichtige Rolle. Im Rahmen ihrer Promotionsarbeiten etablierten die beiden Rossendorfer Wissenschaftler Dr. Robin Steudtner und Dr. Kay Großmann die Fluoreszenzspektroskopie bei tiefen Temperaturen am Helmholz-Zentrum Dresden-Rossendorf (HZDR). Heute, fünf Jahre später, betreut Steudtner am HZDR einen dauerhaften spektroskopischen Tieftemperaturmessplatz zum schnellen und sensitiven Nachweis von Schwermetallen in diversen Umweltproben (Wasser- und Bodenproben). Großmann leitet das Ausgründungsprojekt NanoscopiX am Life Science Inkubator Sachsen.
Reaktionspfade erforschen
Untersuchungen bei tiefen Temperaturen finden breite Anwendung bei elektronenmikroskopischen Methoden, aber auch für fluoreszenzspektroskopische und -mikroskopische Fragestellungen ergeben sich interessante Einsatzgebiete. Die Fluoreszenzausbeute und Fluoreszenzlebensdauer der meisten Fluorophore sind stark temperaturabhängig. Vereinfacht betrachtet, bewirkt das Gefrieren der meist wässrigen Proben, dass die in der Lösung enthaltenen Ionen und Moleküle relativ feste Gitterpositionen in dem gebildeten Wasserkristallgitter einnehmen. Dies reduziert Fluoreszenzlöscheffekte, welche normalerweise bei Raumtemperatur zum Tragen kommen und die Fluoreszenz verringern.
Im Fokus der ersten Arbeiten stand die Erforschung von Reaktionspfaden radioaktiver Schwermetalle in verschiedenen geologischen und biologischen Systemen. Nur aufgrund genauer Kenntnis der Reaktionsmechanismen und der Reaktionspartner der Schwermetallionen lassen sich geeignete Strategien zur Vermeidung gesundheitlicher Risiken und Umweltrisiken entwickeln. Durch den Einsatz der Tieftemperaturtechnik konnte die fluoreszenzspektroskopische Nachweisgrenze für Uran(VI) dabei um mehrere Größenordnungen auf 10-10 M gesenkt werden. Zudem gelang es, die chemische Bindungsform des Urans in verschiedenen natürlichen Medien (Gruben- und Flutungswässer, Mineralwasser und Urin) direkt spektroskopisch zu bestimmen.
Die chemische Bindungsform von Uran kann unter gegebenen chemischen, physikochemischen und physikalischen Parametern mit Hilfe thermodynamischer Berechnungen bestimmt und anschließend mit den experimentellen Ergebnissen verglichen werden. Für die spektroskopische Analyse können die zu untersuchenden Proben ohne weitere Vorbereitung in Plastikküvetten mittels Flüssigstickstoff schockgefroren werden. Nach Überführung der Probe in den Kryostaten wird die spezifische Fluoreszenz des Urans mit einem gepulsten Laser (ʎex = 266 nm)
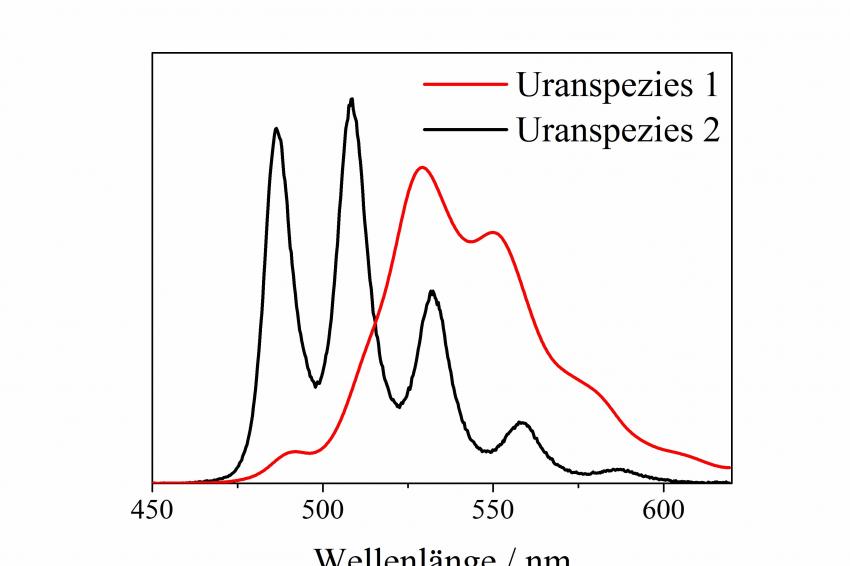
angeregt. Die detektierte Fluoreszenz zeigt im Bereich von 450 nm bis 650 nm das typische Fingerprintspektrum des Uran(VI)-Ions. Die erhaltenen Peakpositionen und die Fluoreszenzlebensdauern sind zwei speziesspezifische Parameter, welche zur Auswertung der Probe genutzt werden. Durch die unterschiedlichen Peaklagen und die unterschiedlichen Fluoreszenzlebensdauern der einzelnen Uranspezies ist unter Einbeziehung der Zeitauflösung eine Analyse von Mehrkomponentensystemen und deren Auftrennung in die Einzelkomponenten möglich (s. Abb. 1).
Je nach Herkunft des einzelnen Probenwassers kann sich die auftretende Uran-Speziation stark unterscheiden. Zum Beispiel zeigt die Speziesverteilung eines realen Grubenwassers aus Königstein (Sachsen), dass in Abhängigkeit vom pH-Wert, fünf chemisch unterschiedliche Uranspezies zum Teil gleichzeitig vorliegen können. In enger Zusammenarbeit zwischen Forschung und Industrie können die so gewonnenen chemischen Erkenntnisse dann anwendungsorientiert der Bewertung und Entwicklung von Sanierungsverfahren für Altlasten des Uranerzbergbaus dienen.
Fluoreszenzmikroskopische Wirkstoffuntersuchungen
Durch die Weiterentwicklung der Fluoreszenzspektroskopie und -mikroskopie bei tiefen Temperaturen werden heute am HZDR nicht nur umweltanalytisch relevante Fragestellungen im Bereich der Radiochemie und Ressourcenökologie sondern auch pharmakologische Fragestellungen im Rahmen der präklinischen Krebsforschung bearbeitet. So werden in enger Zusammenarbeit mit den Doktoranden Christin Wimmer und Christoph Tondera sowie mit Prof. Jens Pietzsch in der Abteilung Radiopharmazeutische und Chemische Biologie am Institut für Radiopharmazeutische Krebsforschung des HZDR fluoreszenzmikroskopische Wirkstoffuntersuchungen an Krebszellen ohne eine spezifische Anfärbung neuer Wirkstoffe durchgeführt.
Durch gezielte Strukturveränderungen, z. B. die Derivatisierung mit einem Fluorophor, wird das Verhalten eines Wirkstoffs in einer Zelle oder im Organismus oft maßgeblich beeinflusst. Die Folge einer derartigen chemischen Modifizierung kann unter anderem ein verändertes Bindungsverhalten des Wirkstoffs an seine Zielmoleküle oder seine veränderte zelluläre Aufnahme sein. Deshalb geht ein Trend hin zur Entwicklung markierungsfreier Analysemethoden.
In einer jüngst veröffentlichten Untersuchung konnte die Eigenfluoreszenz eines, auf der Basis von 2,3-Diaryl-substituierten Indolen neu entwickelten selektiven Cyclooxygenase-2-(COX-2)-Hemmers unter kryogenen Bedingungen genutzt werden, um dessen spezifische Anreicherung direkt an seinem Wirkort auf zellulärer Ebene mikroskopisch und spektroskopisch nachzuweisen (Abb. 2).
Das Enzym COX-2 spielt unter anderem eine wichtige Rolle bei verschiedenen Krebserkrankungen. Eine erhöhte Expression und Aktivität dieses Enzyms führt zu einer krebsfördernden entzündlichen Mikroumgebung, die das Wachstum der Krebszellen verstärkt, ihre Aggressivität erhöht, ihre Immunüberwachung und ihren kontrollierten Zelltod minimiert sowie zur Entwicklung von Resistenzen gegenüber verschiedenen therapeutischen Ansätzen führt.
Zielmolekül adressieren
Das hier beschriebene methodische Herangehen gestattet neben einer pharmakologischen Charakterisierung neuer Wirkstoffe auch Untersuchungen zur funktionellen Charakterisierung dieses Enzyms bei verschiedenen Krebszellen. Beides stellt eine wichtige Voraussetzung dar, um neue Wirkstoffe, die das Enzym COX-2 sowohl für diagnostische als auch für therapeutische Anwendungen als Zielmolekül adressieren sollen, zu entwickeln.
Zum Nachweis verschiedener Stoffwechselprodukte sowie stoffwechselbedingter, chemischer Veränderungen konnte die Methode ebenfalls bereits erfolgreich verwendet werden. So zeigten zum Beispiel spektroskopische Untersuchungen an Laktat, Zitronensäure, Glukose, und Pyruvat Fluoreszenzemissionen bei tiefen Temperaturen, welche bei Raumtemperatur in deutlich geringerem Maße bzw. nicht beobachtet werden konnten. Das untersuchte L-Lactat spielt beispielsweise eine wichtige Rolle als Produkt des anaeroben Abbaus von Pyruvat nach der Glycolyse. Laktat wurde in dieser Studie bei Raumtemperatur, 200 K, 100 K und 10 K untersucht. Dabei konnte bei Raumtemperatur keine Emission beobachtet werden, wohingegen bei 200 K ein auswertbares Spektrum detektiert wurde. Beim weiteren Verringern der Probentemperatur auf 100 K verdoppelte sich die Intensität des Fluoreszenzsignals.
Gegenwärtige Untersuchungen beschäftigen sich mit dem Einfluss des reaktiven Zuckers Glukose auf Lipoproteine geringer Dichte (LDL). Erhöhte Glukosekonzentrationen, wie sie z. B. im Blut von Diabetikern auftreten, führen zur sogenannten Glykatierung von Proteinen und Lipiden (Eiweißen und Fetten). Das sind chemische Veränderungen, die schwerwiegende physiologische Konsequenzen haben können und beispielsweise eng mit den Spätkomplikationen beim Diabetes mellitus Typ 2 im Zusammenhang stehen. Die Glykatierung von LDL steht dabei im Verdacht, bei der Entwicklung atherosklerotischer Blutgefäßveränderungen beteiligt zu sein. LDL und glykatierte LDL (glycLDL) zeigen bei Raumtemperatur und Anregung mit Laserlicht keine ausgeprägten Fluoreszenzeigenschaften. Mit Verminderung der Temperatur wurden für LDL und glycLDL charakteristische und deutlich voneinander abgrenzbare Spektren gemessen. Konzentrationsabhängig konnte in diesen Untersuchungen zudem mit variierender Glukosekonzentration innerhalb der Reaktionslösung eine Abhängigkeit zur Spektrenstruktur festgestellt werden.
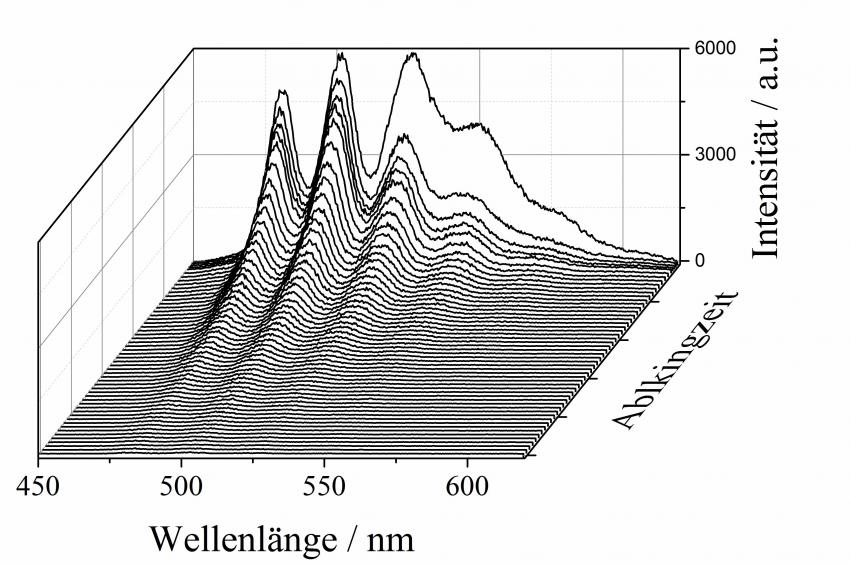
Ähnliche Veränderungen in der Spektrenstruktur wurden auch in Abhängigkeit von der Reaktionsdauer zwischen Glukose und LDL beobachtet (s. Abb. 3). Daraus lassen sich Hinweise auf chemische Veränderungen durch Reaktion der Glukose mit verschiedenen Fett- und Eiweißbestandteilen der LDL ableiten.
Transferorientiertes Folgeprojekt
Auf der Grundlage der bisherigen Untersuchungen und Ergebnisse am HZDR wurde erfolgreich das transferorientierte Folgeprojekt „NanoscopiX" am Life Science Inkubator Sachsen initiiert. NanoscopiX beschäftigt sich dabei mit der applikationsbezogenen Weiterentwicklung der Tieftemperaturfluoreszenzmikroskopie und -spektroskopie. Dabei ist das vorrangige Ziel, ein einfach zu handhabendes, sensitives analytisches Verfahren für chemo- , bioanalytische- und medizinische Anwendungen zu entwickeln.
Die Analyse von Schwermetallen, insbesondere von Radionukliden und seltenen Erden in natürlichen Systemen, soll an Hand einer verbesserten Fluoreszenzanalytik bei tiefen Temperaturen erweitert werden.
Mit Unterstützung der Max-Buchner-Forschungsstiftung konnten drei entscheidende Ergebnisse erzielt werden, welche für zukünftige Projekte die nötige wissenschaftliche Grundlage bieten.
• Aufbau eines dauerhaften spektroskopischen Tieftemperaturmessplatzes zum schnellen und sensitiven Nachweis von Uran in diversen Umweltproben (Wasser- und Bodenproben)
• Unterstützung beim Aufbau eines mikroskopischen Tieftemperaturmessplatzes, der mikroskopische Untersuchungen bei -253 °C mit bis zu 630-facher Vergrößerung erlaubt
• Erste erfolgreiche Untersuchungen am spektroskopischen und mikroskopischen Messplatz im Bereich der Umweltanalytik sowie zu verschiedenen medizinisch relevanten Fragestellungen
Langfristig zielen die Arbeiten auf die direkte Visualisierung der Analyten bei tiefen Temperaturen in biologischen und medizinischen Proben in Kombination mit fluoreszenzspektroskopischen Daten, welche zusätzliche molekulare Informationen über die Mikroumgebung der Fluorophore liefern, ab.