Arsen in der Umwelt
Extraktion von Arsenspezies aus der Braunalge Undaria Pinnatifida (Wakame)
Arsen kommt in der Natur ubiquitär vor. Man findet es im Boden, im Wasser, in der Luft und auch in unserer Nahrungskette. Die größten Mengen an Arsen nimmt der Mensch durch den Verzehr von Meeresfrüchten und durch kontaminiertes Trinkwasser auf. Man schätzt, dass mehr als 100 Millionen Menschen auf der Welt arsenbelastetes Wasser trinken. Mehrere Studien bewiesen schon, dass Meeresfrüchte und Fische mitunter einen hohen Arsengehalt aufweisen können. Arsen kommt dann meist in Form der organischen Arsenverbindungen vor, die im Gegensatz zu anorganischen Arsenverbindungen eine geringere Toxizität aufweisen. Algen spielen in diesen Zusammenhang eine wichtige Rolle.
Algen dienen besonders in Japan, mittlerweile auch in europäischen Ländern als Nahrungsmittel. Sie besitzen die Eigenschaft, die im Meerwasser enthaltenen anorganischen Arsenverbindungen in großen Mengen aufzunehmen und diese dann in organische Arsenverbindungen umzuwandeln und zu speichern [1]. Der Arsengehalt in Algen schwankt zwischen 1,4 und 62 mg/kg. In tierischen Meeresorganismen kommen die organischen Arsenverbindungen wie Arsenobetain, Dimethylarsinsäure (DMA), Monomethylarsonsäure (MMA), Tetramethylarsoniumion TMAs+, Trimethylarsinoxid (TMAO), Arsenocholin (AsC) vor und in pflanzlichen Meeresorganismen treten vorwiegend Arsenozucker auf [2]. Algenerzeugnisse wie die Braunalge Wakame besitzen einen hohen Iodgehalt (104 - 350 mg/kg) und die Fähigkeit Arsen in großen Mengen aus dem Meerwasser aufzunehmen und zu speichern [3]. Die Zellwand der Braunalgen besteht aus einer festen fibrillären (Cellulose) und einer amorphen Fraktion (unlösliches Alginat) [4]. Braunalgen kommen z. B. in Form der Wakame, Hijiki oder Kombu auf den Markt [11]. Die Braunalge Wakame enthält besonders viel Alginat, dass bei der Extraktion der Arsenspezies aus dieser Alge zu Problemen hinsichtlich der Extrahierbarkeit und der Reproduzierbarkeit führt. Die Alginsäure bzw. deren Salze bilden wasserunlösliche Gele, die Arsenspezies sorbieren oder kovalent binden können. Unterschiedliche Kationen führen dabei zu mehr oder weniger löslichen Alginaten. So sind die mit zwei - oder mehrwertigen Kationen (Ausnahme Magnesiumalginat) wasserunlöslich, wobei sich Natrium -, Kalium - und Ammoniumalginat gut in Wasser lösen. In Braunalgen findet man meist folgende Kationen als Gegenionen: Na+, K+, Mg2+, Ca2+, Sr2+ und Ba2+. Alginate werden den hydrophilen Kolloiden zugeordnet, d. h dass die kolloidal gelösten Verbindungen überwiegend durch Umhüllung von Wassermolekülen stabilisiert werden [5]. Im Allgemeinen werden Alginate dort industriell verwendet, wo Suspensionen und Emulsionen stabilisiert werden müssen [6].
Ziel dieser Arbeit war es, die existierenden Arsenspezies in der Braunalge Undaria pinnatifida (Wakame) über schonende Extraktionsverfahren zu extrahieren und mittels HPLC (IC) - ESI/Massenspektrometrie zu identifizieren. Zusätzlich sollen quantitative Aussagen bezüglich der Extrahierbarkeit und der Chromatographierbarkeit der Arsenspezies gemacht werden.
Experimentelles
Extraktionsmittel
Als Extraktionsmittel wurden folgende Chemikalien verwendet: NaOH (10 - 50 mM), Na2CO3 (20 mM), Methanol und destilliertes Wasser.
Probe
Für diese Arbeit wurde eine handelsübliche, getrocknete Braunalge Wakame genutzt, die fein gemahlen und bei ca. 7 °C gelagert wurde. Zur mikrowellenunterstützten Extraktion diente die Mikrowelle Multiwave (Perkin Elmer). Die Schüttelextraktionen wurden an einem Horizontalschüttler durchgeführt.
Instrumentelles
Arsengesamtgehalt in der Feststoffprobe: RFA (Spectro X - Lab 2000, Spectro). Die ermittelte Arsenkonzentration von 46 ± 4,6 mg/kg wurde als Referenzwert verwendet.
Arsengesamtkonzentration im Extrakt: ICPMS (ELAN DRC - e, MDS SCIEX).
Chromatographie: HPLC - Series 1100 (Agilent) mit Degasser und Autosampler; Detektion mittels ICP - MS (7500 ce, Agilent) und parallel mit ESI - MS (MSD 6130, Agilent).
Trennsäule: IonPac AS7/AG7 (Dionex)
Eluent: Eluent (A) : H2O/MeOH (1 %); Eluenwt (B): NH4HCO3 (20 mM, pH 10)/MeOH (1 %).
Ergebnisse und Diskussion
Zur Optimierung der schonenden Extraktion von Arsenspezies aus der Wakame - Alge wurden alkalische Elutionsmittel mit Na+ als Kation eingesetzt. Mit diesen Extraktionsmitteln sollte es möglich sein, die zweiwertigen Kationen z. B. Ca2+ aus dem Alginat zu substituieren, um somit das Alginat in Lösung zu bringen. Zum anderen wurde eine chromatographische Trennmethode ausgewählt, die das Ausfallen der Alginsäure im sauren Medium unterdrückt. Die o.g. chromatographische Analyse erlaubt die Trennung von anorganischen und organischen Arsenverbindungen innerhalb von 35 min. Die parallele Kopplung der beiden Detektoren ICP-MS und ESI-MS diente der Zuordnung der einzelnen Arsenspezies mittels Detektion auf m/z 75 As (ICP/MS) zu den simultan-detektierten Massenspektren, die mittels ESI/MS (Scan-Modus, positive Ionisierung) erhalten werden und zur Strukturaufklärung der Arsenspezies verwendet wurden. [7]
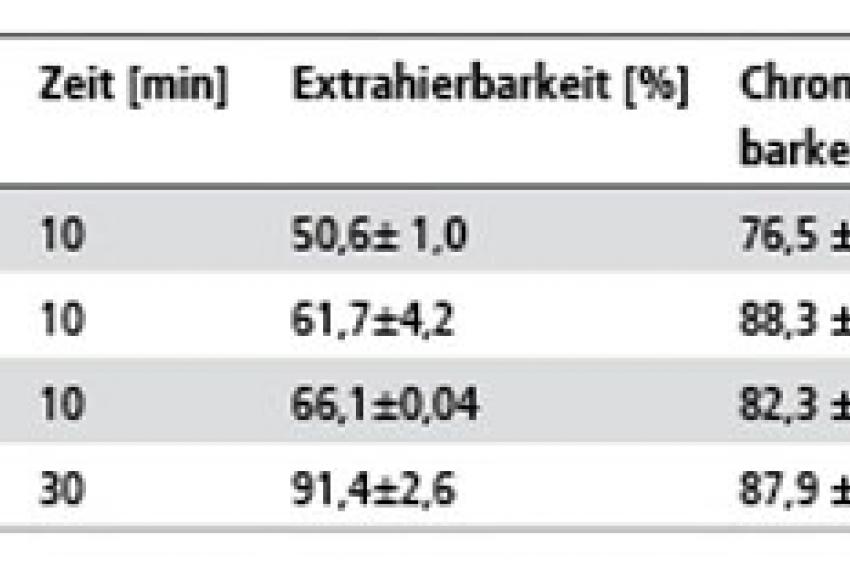
Zur Quantifizierung der Extraktionsausbeute wird die Extrahierbarkeit (E) berechnet (Abb.1). Die Extrahierbarkeit ist der prozentuale Arsengehalt im Extrakt bezogen auf den Arsengehalt im Feststoff. Er wird als maximal möglicher Arsengehalt in der Wakame - Probe zu 100 % gesetzt. Der Arsengehalt im Extrakt wird ins Verhältnis zum RFA-Gesamtgehalt gesetzt. Darüber hinaus gibt der Parameter Chromatographierbarkeit (C) an, wie viel der extrahierten Spezies unter den gegebenen chromatographischen Bedingungen auch chromatographierbar sind. Die Chromatographierbarkeit ist der prozentuale Arsengehalt im Extrakt nach einer Chromatographie bezogen auf den Arsengehalt im Extrakt ohne Chromatographie. Der Arsengehalt im Extrakt nach der Chromatographie wurde mit der HPLC - ICP/MS -Messung ermittelt. Er ergibt sich aus der Summe der Konzentrationen aller chromatographierbaren Arsenspezies. Der Gesamtarsengehalt im Extrakt wurde mittels ICP/MS analysiert. Er ist der maximal mögliche Arsengehalt im Extrakt (Summe der Konzentrationen aller extrahierten Arsenspezies) und wird zur Ermittlung der Chromatographierbarkeit zu 100 % gesetzt. (Abb.1). Die mikrowellenunterstützte Extraktion wurde bei verschiedenen Temperaturen und zwei Extraktionszeiten (Tab. 1) durchgeführt. Die höchsten Extrahier- und Chromatographierbarkeiten von ca. 90 % werden bei Temperaturen von 150°C und 30 min erzielt. Vergleicht man die Chromatogramme der mikrowellenunterstützten Extraktion mit Wasser mit der von 20 mM NaOH (Abb.2), so kann Folgendes geschlussfolgert werden:
- Die Konzentration der wasserextrahierten Arsenspezies (Peakintensität) ist wesentlich geringer als mit NaOH extrahierte.
- Die Anzahl der chromatographierten Arsenspezies ist in beiden Chromatogrammen gleich.
- Die Wasserextraktion führt hauptsächlich zu Glycerol-AsZ, DMA und Arsenat.
- Mit der NaOH-Extraktion werden hohe Peakintensitäten für 4 Arsenozucker, Dimethylarsinoylacetat und Arsenat erhalten.
- Unbekannte Peaks z. B. [M+H]+ m/z 391, 2 benachbarte Peaks mit der Masse [M+H]+ m/z 409 und weitere mit geringer Intensität (Peaks 8) werden detektiert.
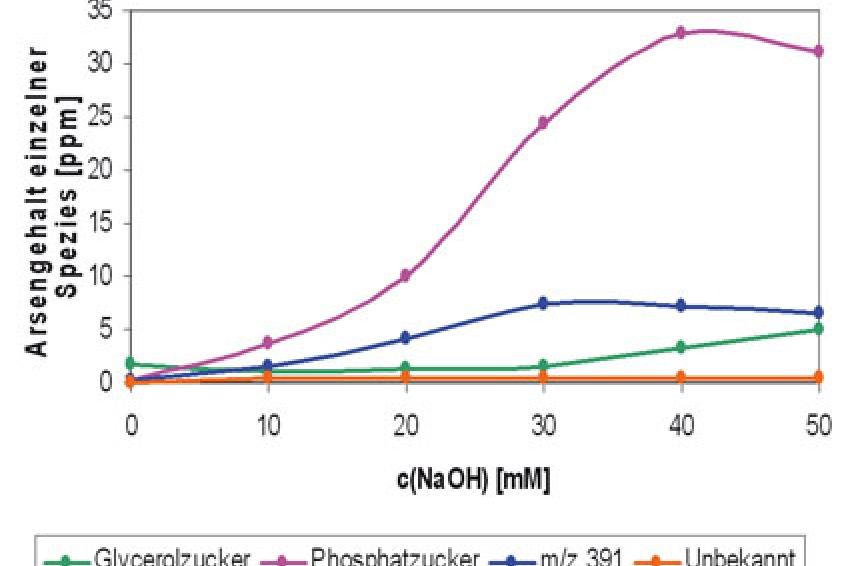
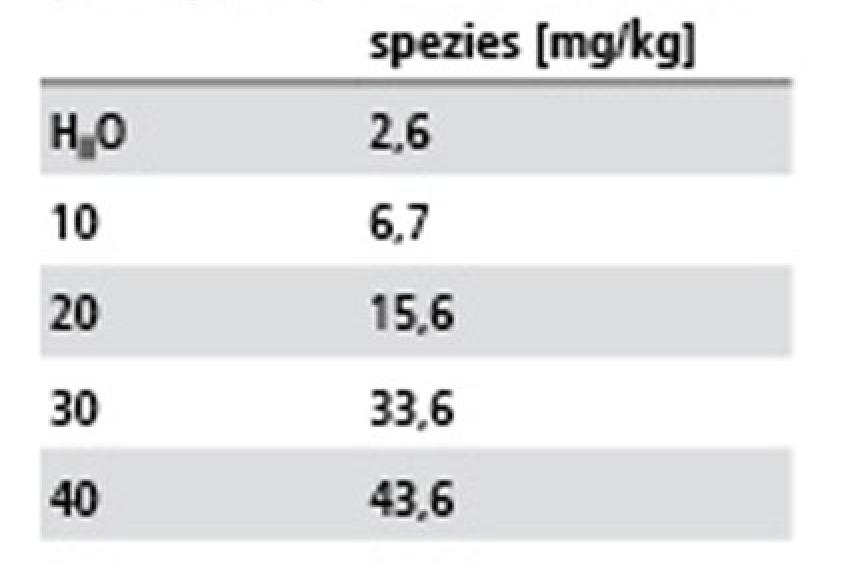
Aber auch bei der Schüttelextraktion (24 h) kann man durch Erhöhung der NaOH-Konzentration im Bereich von 10 - 50 mM die Extrahierbarkeit und Chromatographierbarkeit (Tab. 2) steigern. Die Summe der Arsenspezies-Konzentration ergibt bei einer NaOH-Konzentration von 50 mM einen Wert von 43,1 mg/kg, was einer Extraktionsausbeute von 94 % bezogen auf den Referenzwert von 46 mg/kg entspricht. Welche Arsenspezies an der Erhöhung der Extraktionsausbeute in Abhängigkeit von der NaOH-Konzentration beteiligt sind, wird aus Abb. 3 ersichtlich. Besonders trägt der Phosphat - AsZ zur Erhöhung der Extraktionsausbeute bei, gefolgt von der unbekannten Komponente (m/z 391) und ab 30 mM NaOH auch vom Glycerol-AsZ.
Es ist bekannt, dass die Alginsäure auf Grund ihrer Hydroxyl- und Carboxylgruppen Ester bilden kann. Ein Bespiel dafür ist das Propylenglycolalginat (E405). Es könnte auch der Phosphat-AsZ mit dem Alginat verestert vorliegen. Durch alkalische Verseifung mit steigender NaOH-Konzentration würde der Arsenozucker in Lösung gehen und extrahiert werden können. Ähnliches kann man sich auch für andere Arsenozucker vorstellen. Auch der „freie" Phosphat-AsZ kann weiter verseift werden und könnte zum einen in Glycerol-AsZ und die entsprechende Phosphonsäure zerfallen oder zum anderen den Polyalkohol abspalten. Letzteres würde zu einem Phosphat-AsZ(3) mit der m/z 391 führen, der in Abbildung 2 als Peak 4 auftritt.
Wie in Abb. 2 und Tab. 3 gezeigt, treten auch Peaks mit gleichem Masse/Ladungsverhältnis auf (z. B. m/z 409), was darauf hindeutet, dass verschiedene Arsenozucker die gleiche Molmasse besitzen und demzufolge zu unterschiedlichen Zeiten retardieren.
Zusammenfassung
Eine Methode zur besseren Extrahierbarkeit von As-Spezies in Algen wurde entwickelt und für die Extraktion der Wakame - Alge genutzt.
Hohe Extraktionsausbeuten wurden erzielt mit:
- 30 - 50 mM NaOH für die Schüttelextraktion bzw. T=150 °C, t=30 min in der Mikrowelle.
- Hohe Chromatographierbarkeiten konnten erreicht werden mit einem alkalischen Eluenten und einer Anionenaustauschsäule.
- Die Identifizierung bekannter und unbekannter As-Spezies wurde durch den Vergleich der ICP/MS- und ESI/MS-Detektion möglich.
Literatur
[1] Chen Yang; Donghwa Chung; SangGuan You: Food Chemistry 111, 503-507 (2008)
[2] Wuilloud, R. G.; Altamirano, J. C.; Smichowski, P. N.; Heitkemper; D. T.: J. Anal. At. Spectrom. 21 1221 (2006)
[3] Thomson, D.; Maher, W.; Forster, S.: Appl. Organometal. Chem. 21396-411 (2007)
[4] van den Hoek, Ch.; Jahns, H. M.; Mann; D. G.:
Algen, Georg Thieme Verlag Stuttgart, 1993, 136 (ISBN 3-13-551103-0)
[5] Marburger; A.: Alginate und Carrageenane - Eigenschaften, Gewinnung und Anwendungen in Schulen und Hochschulen, Dissertation, Marburg/Lahn 7-13 (2003)
[6] Rinaudo, M.: Seaweed polysaccharides in Comprehensive Glycoscience (ed. J.P. Kamerling, Elsevier) Vol. 2, 691-735
[7] Mattusch, J.; Möller, D.; Elizalde-Gonzalez, M. P.; Wennrich, R.: Anal. Bioanal. Chem. 390/71707-1715 (2008)
Kontakt
Helmholtz-Zentrum für Umweltforschung - UFZ
Permoserstr
04318 Leipzig
Deutschland
+49 341 235 1635
+49 341 235 1468